Un atom este o particulă minimă integrală a materiei. În centrul său se află un nucleu, în jurul căruia, precum planetele din jurul soarelui, se învârtesc electroni. Ciudat, dar această particulă cea mai mică a fost descoperită și a formulat conceptul

cercetători antici greci și antici din India, care nu au echipamentul sau baza teoretică corespunzătoare. Calculele lor timp de mai multe secole au existat pe baza ipotezelor și abia în secolul al XVII-lea, oamenii de știință chimici au putut să dovedească experimental validitatea teoriilor antice. Dar știința avansează rapid, iar la începutul secolului trecut, fizicienii au descoperit componente subatomice și structuri de particule. Atunci a fost respinsă o astfel de definiție a atomului drept „indivizibil”. Cu toate acestea, conceptul a intrat deja în uz științific și a fost păstrat.
Oamenii de știință antici credeau că atomul este cea mai mică bucată din orice materie. Proprietățile fizice ale unei substanțe depind de forma, masivitatea, culoarea și alți parametri. De exemplu, Democritus credea că atomii de foc sunt extrem de ascuțiți, pentru că arde, particulele de solide au suprafețe dure, care se atașează strâns unul de celălalt, atomii de apă sunt netede și alunecoase, deoarece dau fluiditate fluidității.

Democrit considera chiar că sufletul omului este alcătuit din atomi conectați temporar, care se descompun atunci când individul moare.
O structură mai modernă a fost propusă la începutul secolului XX de către fizicianul japonez Nagaoka. El a prezentat dezvoltarea teoretică, care constă în faptul că atomul este un sistem planetar la scară microscopică, iar structura sa este similară cu cea a lui Saturn. O astfel de structură s-a dovedit eronată. Modelul atomului Bohr-Rutherfried s-a dovedit a fi mai aproape de realitate, dar chiar ea nu a reușit să explice toate proprietățile fizice și electrice ale corpusculilor. Numai ipoteza că un atom este o structură care include nu numai proprietățile corpusculare, ci și cele cuantice, ar putea explica cel mai mare număr de realități observate.
Corpusculele pot fi într-o stare legată sau pot fi într-o stare liberă. De exemplu, un atom de oxigen, pentru a forma o moleculă, se combină cu o altă particulă similară. După o descărcare electrică, cum ar fi furtuna, se combină
o structură mai complexă este azina, care este formată din molecule triatomice. În consecință, anumite condiții fizice și chimice sunt necesare pentru un anumit tip de compuși atomici. Dar există legături mai puternice între particulele moleculei. De exemplu, un atom de azot este conectat la o altă legătură triplă, ca urmare, molecula este extrem de puternică și aproape neschimbată.
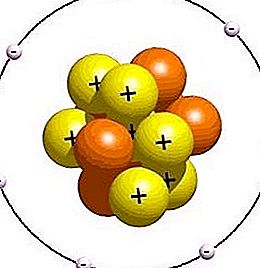
Dacă numărul protonilor (particule elementare ale nucleului) este similar cu numărul de electroni care se rotesc pe orbite, atunci atomul este neutru electric. Dacă nu există identitate, atunci particulele au o descărcare negativă sau pozitivă și se numește ion. De regulă, aceste particule încărcate sunt formate din atomi sub influența câmpurilor electrice, radiații de natură variată sau temperaturi ridicate. Ionii sunt hiperactivi chimic. Acești atomi încărcați sunt capabili să reacționeze dinamic cu alte particule.




